Die Leber ist die größte Drüse des menschlichen Körpers. Sie befindet sich im rechten oberen Quadranten des Abdomens und wiegt etwa 1,5 Kilogramm. Hauptfunktionen der Leber sind Entgiftung, Stoffwechsel ( Kohlenhydrate Kohlenhydrate Chemie der Kohlenhydrate, Proteine Proteine Proteine und Peptide, Lipide Lipide Fettsäuren und Lipide, Hormone Hormone Endokrines System: Überblick), Nährstoffspeicherung (z. B. Eisen Eisen Spurenelemente und Vitamine), Synthese von Gerinnungsfaktoren, Gallenproduktion, Filtration und Blutspeicherung. Die Leber kann in 4 Lappen oder in 8 Segmente unterteilt werden. Mikroskopisch ist eine Unterteilung in Leberläppchen erkennbar. Das wichtigste Gefäß-Nerven-Bündel der Leber verläuft in der Querfissur der Leber und enthält die Pfortader.
Kostenloser
Download
Lernleitfaden
Medizin ➜
Die Leber ist die größte Drüse des Körpers. Sie erstreckt sich von der rechten bis zur linken Regio hypochondriaca (¾ der Leber liegt im rechten oberen Quadranten des Abdomens).

Lage der Leber in der Bauchhöhle
Bild von Lecturio.
Frontalansicht der Bauchhöhle mit entfernter Leber. Die Abbildung zeigt die Lage der Leber in der Bauchhöhle im Verhältnis zu benachbarten Organen.
Bild von Lecturio.
Topographie der Leber
Bild von Lecturio.
Ansicht von inferior auf die Facies visceralis der Leber. Beachten Sie die ungleichmäßige Struktur, die durch Abdrücke der Nachbarorgane entsteht. Die Impressio colica wird durch die Flexura coli dextra des Dickdarms verursacht; die Impressio duodenalis ist auf den Pars descendens des Duodenums zurückzuführen.
Bild von Lecturio.
Acht Lebersegmente nach dem Couinaud-Klassifikationssystem
Bild von Lecturio.Die Leberpforte ist eine transversale Fissur Fissur Generalisierte und lokalisierte Exantheme zwischen dem Lobus caudatus und dem Lobus quadratus, die als Durchgang für folgende Strukturen dient:

Ansicht von inferior auf die Facies visceralis der Leber mit der Leberpforte und dem umgebenden Ligamentum hepatuduodenale
Bild von Lecturio.Definition: Die Ligamente der Leber sind Duplikaturen des Peritoneum Peritoneum Peritoneum und Retroperitoneum viscerale, die die Leber in ihrer Umgebung verankern.
|
Ligamentum coronarium |
Peritoneale Umschlagsfalte vom
Diaphragma
Diaphragma
Zwerchfell (Diaphragma) auf die Leber Begrenzung der Area nuda (Leberoberfläche ohne Peritonealbedeckung) |
| Ligamentum falciforme |
Bauchfellduplikatur der Vorderfläche der Leber und der Rückfläche der Bauchwand Überbleibsel des embryonalen ventralen Mesenteriums Der freie Rand enthält das Ligamentum teres hepatis. |
| Ligamentum hepatuduodenale |
Teil des Omentum minus Erstreckt sich von der Porta hepatis bis zum oberen Teil des Duodenums Inhalt: A. hepatis propria, Pfortader, Ductus hepaticus communis |
| Ligamentum hepategastricum |
Erstreckt sich von der Leber bis zur kleinen Kurvatur des Magens Inhalt: Aa. gastricae |
|
Ligamentum teres hepatis |
Überbleibsel des intraabdominalen Anteils der Nabelvene Erstreckt sich vom Nabel bis zur Leber am freien Rand des Ligamentum falciforme |
| Ligg. triangularia |
Verschmelzung der vorderen und hinteren Falte des Ligamentum coronarium Links und rechts; beide erstrecken sich von der Leber bis zum Diaphragma Diaphragma Zwerchfell (Diaphragma) |
|
Ligamentum venosum |
Überbleibsel des Ductus venosus Erstreckt sich vom Überbleibsel des intraabdominalen Teils der Nabelvene bis zur V. cava inferior |
| Linke Fissur Fissur Generalisierte und lokalisierte Exantheme | Impressionen des Ligamentum teres hepatos und venosum |
| Rechte Fissur Fissur Generalisierte und lokalisierte Exantheme | Impressionen der Gallenblase Gallenblase Gallenblase und Gallenwege und der V. cava inferior |

Vorderansicht der Facies diaphragmatica der Leber mit dem Lig. falciforme, Ligg. triangularia, Lig. teres hepatis und Lig. coronarium. Beachten Sie, dass sich das Lig. teres hepatis vom freien Rand des Ligamentum falciforme aus erstreckt.
Bild von Lecturio.
Vorderansicht der Leber. Die Leber wurde angehoben, um das Omentum minus darzustellen, das sich aus dem Ligamentum hepatogastricum und hepatoduodenale zusammensetzt. Diese Duplikatur des Peritoneums verbindet die Leber mit der kleinen Kurvatur des Magens und dem Duodenum.
Bild von Lecturio.
Anterosuperiore Ansicht einer menschlichen Leber
Bild : “Hypoplastic left lobe of liver with accessory caudate lobe.” von Department of Anatomy, AIIMS, Rishikesh, Uttarakhand 249201, Indien. Lizenz: CC BY 3.0
Posteroinferiore Ansicht einer Leber
Bild : “Hypoplastic left lobe of liver with accessory caudate lobe.” von Department of Anatomy, AIIMS, Rishikesh, Uttarakhand 249201, Indien. Lizenz: CC BY 3.0
Schematische Darstellung des Aufbaus eines Leberläppchens. Die Glisson-Trias an den Eckpunkten besteht aus Ästen der V. portae hepatis, der A. hepatica propria und einem Gallengang. Der Ast der V. portae hepatis führt nährstoffreiches, aber sauerstoffarmes Blut aus dem Dünndarm. Der Ast der A. hepatica propria versorgt die Hepatozyten mit sauerstoffreichem Blut. Der Gallengang leitet Galle von den Hepatozyten in Richtung größerer Gallengänge und der Gallenblase ab.
Bild von Lecturio.
Schematische Darstellung der drei Arten von Lebereinheiten. Beachten Sie die Periportalfelder an den Scheitelpunkten der hexagonalen Leberläppchen und die drei histologischen Zonen innerhalb des Leberazinus.
Bild von Lecturio.
Schematische Darstellung eines Sinusoids und eines Leberbälkchens, die durch den Disse-Raum getrennt sind. Beachten Sie die spezialisierten Zellen der Leber: Kupffer-, Pit- und Ito-Zellen.
Bild von Lecturio.
Schematische Darstellung der Histologie der Leber. Beachten Sie, dass die V. interlobularis durch das weite Lumen und die dünne Wand der glatten Muskelzellen identifiziert werden kann. Die A. interlobularis weist ein engeres Lumen auf und ist von einer dickeren Schicht glatter Muskulatur umgeben. Die Wände des Gallengangs enthalten quaderförmige Epithelzellen (Cholangiozyten), die eine Unterscheidung von der A. interlobularis ermöglichen.
Bild von Lecturio.
Histologischer Schnitt durch das Lebergewebe mit Sinusoid (1), diskontinuierlicher Basallamina (2), gefenstertem Endothel (3) und dem perisinusoidalen Disse-Raum (4).
Bild von Lecturio.
Histologischer Schnitt durch das Lebergewebe mit einer Zentralvene (oben) und einem Periportalfeld (unten).
Bild von Lecturio.Die Leber weist eine spezielle, duale Blutversorgung auf. Sie enthält eine Mischung aus sauerstoffreichem, sauerstoffarmem und nährstoffreichem Blut.

Übersicht über die arterielle Durchblutung des Abdomens. Der Truncus coeliacus ist der erste Hauptast der Aorta abdominalis. Er versorgt Leber, Magen, Milz, Pankreas sowie Teile des Ösophagus und des Duodenums mit sauerstoffreichem Blut. Der Truncus coeliacus gibt die A. gastrica sinistra, die A. splenica und die A. hepatica communis ab. Die A. hepatica communis teilt sich in die A. hepatica propria, die A. gastroduodenalis und die A. gastrica dextra, die in der Abbildung dargestellt sind.
Bild von Lecturio.
Schematische Darstellung des venösen Portalsystems. Die Pfortader wird am häufigsten durch die Vereinigung der V. splenica und der V. mesenterica superior gebildet. Direkte Zuflüsse sind die V. mesenterica inferior, V. cystica, V. gastrica dextra und sinistra. Insgesamt sammelt das Portalsystem den venösen Abfluss der Milz, des Magens, der Gallenblase, des Dünn- und Dickdarms und des Pankreas.
Bild : “Hepatic Portal Vein System” von OpenStax College. Lizenz: CC BY 3.0Nodi lymphoidei hepatici (an der Leberpforte) → Nodi lymphoidei coeliaci → Cisterna chyli (sackförmige Erweiterung der Lymphgefäße, die Lymphe aus dem Magen-Darm-Trakt und den Trunci lumbales aufnimmt→ Ductus thoracicus
Canaliculi biliferi → Ductuli biliferi interlobulares → Ductus hepaticus dexter und Ductus hepaticus sinister → Ductus hepaticus communis → Ductus choledochus → Duodenum Duodenum Dünndarm
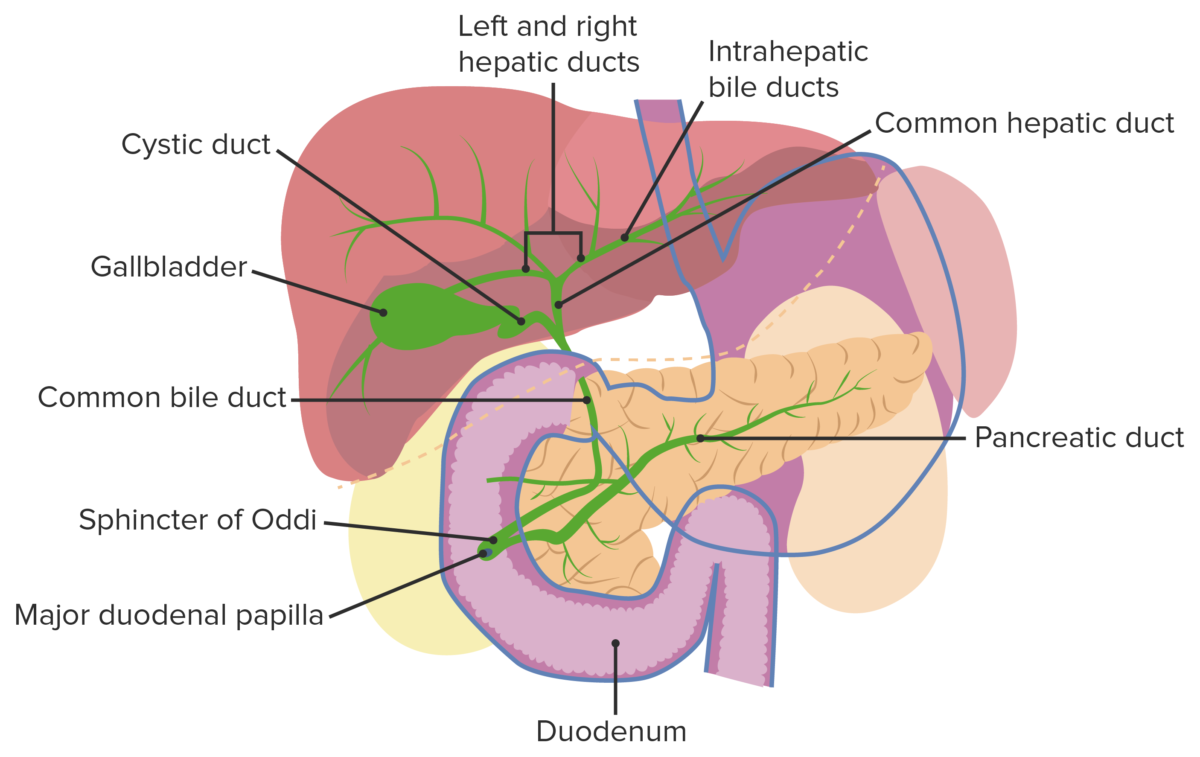
Gallenblase und Gallenwege
Bild von Lecturio.Die Leber eliminiert Abbauprodukte, die durch Resorption aus dem Gastrointestinaltrakt entstehen. Durch enzymatische Modifikation werden fettlösliche Stoffe in wasserlösliche Substanzen umgewandelt. Dies ermöglicht eine Ausscheidung über die Gallenwege Gallenwege Gallenblase und Gallenwege oder über den Urin.

Schematische Darstellung der verschiedenen Stoffwechselwege, an denen die Leber beteiligt ist
Bild von Lecturio.Neoplasien
Infektionen
Entzündliche Erkrankungen
Genetische Erkrankungen
Weitere Erkrankungen