Mukoviszidose, auch zystische Fibrose (englisch: Cystic Fibrosis) genannt, ist eine autosomal-rezessiv vererbte Erkrankung, die durch Mutationen im CFTR-Gen verursacht wird. Die Mutationen verursachen eine Dysfunktion der Chloridkanäle, was zu hyperviskosem Schleim und einer Ansammlung von Sekret in verschiedenen Organen führen kann. Häufige Symptome sind chronische Atemwegsinfektionen, Gedeihstörungen und eine Pankreasinsuffizienz. Der Goldstandard für die Diagnostik ist der Schweißchloridtest, der durch Gentests ergänzt werden kann. Mukoviszidose führt letztendlich zu chronischen Entzündungen und einem Multisystemorganversagen. Die Therapie kann zum Teil kausal unter Anwendung von CFTR-Modulatoren erfolgen. Weitere wichtige Therapiesäulen stellen Sekretolyse, Physiotherapie und antibiotische Behandlung als supportive Maßnahmen dar. Ultima ratio ist die Lungentransplantation Lungentransplantation Organtransplantation. Die Prognose variiert je nach Behandlung und Komplikationen. Bei optimaler medizinischer Versorgung können Betroffene im Schnitt das 53. Lebensjahr erreichen.
Kostenloser
Download
Lernleitfaden
Medizin ➜

Mutationsarten bei Mukoviszidose
Bild von Lecturio.Auswirkungen auf Organsysteme
| Dünndarm Dünndarm Dünndarm | Dicke Sekrete beeinträchtigen die Resorption und erhöhen das Risiko einer Obstruktion. |
|
| Dickdarm Dickdarm Colon, Caecum und Appendix vermiformis | Unvollständig verdaute Makronährstoffe führen zu dickem Stuhlgang und prädisponieren den Patienten für Impaktion, Obstruktion und Invagination Invagination Invagination. | |
| Pankreas Pankreas Pankreas: Anatomie und Funktion |
|
Bauchschmerzen; Bauchkrämpfe; Blähungen; häufiger voluminöser, öliger Stuhlgang; Gewichtsverlust; Blähung |
| Hepatobiliär |
|
Schmerzen im rechten oberen Quadranten nach großen, fettigen Mahlzeiten; Brechreiz; Erbrechen Erbrechen Erbrechen im Kindesalter; Gelbsucht |
Um sich an die häufigsten klinischen Merkmale der Mukoviszidose zu erinnern, erinnern Sie sich an das Akronym CF PANCREAS:
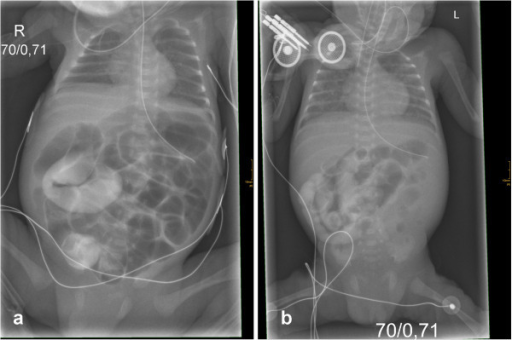
Ein tödlich verlaufender Mekoniumileus bei Frühgeborenen, der eine neuartige Mukoviszidose-Mutation aufdeckt
Bild: “Initial X-rays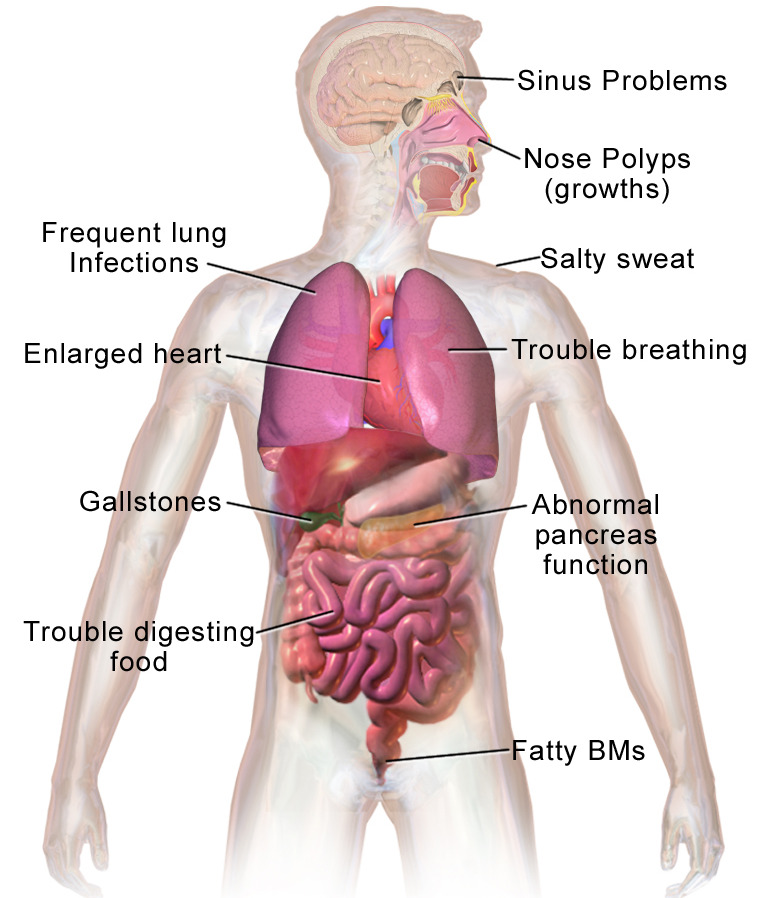
Die häufigsten Kliniken von Mukoviszidose
BMs: Stuhlgang
| Verschlimmerung einer Lungenerkrankung |
|
|---|---|
| Chronische mikrobielle Besiedlung |
|
| Allergische bronchopulmonale Aspergillose Aspergillose Aspergillus/Aspergillose | Besiedelung der Atemwege mit Aspergillus, gefolgt von einer starken IgE- und IgG-vermittelten Immunantwort, unterschiedliche Erscheinungsformen, die eine Verschlimmerung des Fiebers, Unwohlsein, Schleimverstopfung umfassen können, die sich mit Antibiotika möglicherweise nicht bessert |
| Biliäre Zirrhose | Gallengangsobstruktion bei Erwachsenen |
| Endokrine Pankreasinsuffizienz | Entwicklung von Diabetes mellitus Diabetes Mellitus Diabetes Mellitus, einschließlich Zerstörung der Langerhans-Inseln im Erwachsenenalter |

Testalgorithmus für CF, wie er in vielen Ländern durchgeführt wird. IRT: immunreaktives Trypsinogen
Bild von Lecturio.
Prinzip und Durchführung eines Schweißchloridtests
Bild von Lecturio.Bleibt die Diagnose unklar, können weitere Untersuchungen durchgeführt werden.
Nasale Potentialdifferenz
Fäkale Elastase
Eine Pankreasinsuffizienz kann beim Screening des Stuhls auf Pankreas-Elastase-1 festgestellt werden, die bei 80 % der Menschen mit CF fehlt.
Bildgebung
Nachweis von Mikroorganismen in den Atemwegen
Die Behandlung von CF sollte multidisziplinär sein und spezialisierte Ärzte, Physiotherapeuten, Ernährungsberater und/oder psychologische Unterstützung umfassen.
| Organsystem | Therapieansatz |
|---|---|
| Lungeninfektionen, respiratorische Lungeninsuffizienz |
|
| Hypotone Dehydratation/hypochlorämische Alkalose |
|
| Exokrine Pankreasinsuffizienz | Eine Dosis Pankreasenzyme (definierte Lipase- und Proteasekonzentration) zu jeder Mahlzeit |
| Gedeihstörung Gedeihstörung Gedeihstörung |
|
| Vitamin- und Mineralstoffmangel | Prophylaktische Substitution fettlöslicher Vitamine in übernormaler Dosierung, Ersatz von Mineralstoffen und Spurenelementen |
| CF-bedingter Diabetes Diabetes Diabetes Mellitus |
Die folgenden Erkrankungen stehen im Zusammenhang mit Mukoviszidose: