Das humane Immundefizienz-Virus ( HIV HIV Retroviren: HIV), ein einzelsträngiges RNA-Virus aus der Familie der Retroviridae. Es gilt als der ätiologische Erreger des Acquired Immunodeficiency Syndrome (AIDS). HIV HIV Retroviren: HIV ist eine sexuell oder durch Blut übertragbare Infektion, die CD4+-T-Lymphozyten, Makrophagen Makrophagen Zellen des angeborenen Immunsystems und dendritische Zellen angreift und schließlich zu einem Immundefekt führt. Die Klinik ist durch konstitutionelle Symptome wie Lymphadenopathie Lymphadenopathie Lymphadenopathie und Fieber Fieber Fieber gekennzeichnet. Seine Progression prädisponiert für opportunistische Infektionen und Malignome. Die Diagnose erfolgt durch Antikörpersuchtests für HIV-1 und -2. Zusätzliche Untersuchungen der HIV-Viruslast, die Genotypisierung und die CD4+-T-Lymphozytenzahl werden genutzt, um die richtige Therapie zu festzulegen und das Ansprechen auf die Therapie sowie das Fortschreiten der Erkrankung zu beurteilen. Eine sofortige Therapie mit einer antiretroviralen Therapie (ART) wird empfohlen.
Kostenloser
Download
Lernleitfaden
Medizin ➜

Weltkarte der HIV-Infektionen 2017 (von Personen im Alter von 15-49 Jahren):
Der Prozentsatz der mit dem humanen Immundefizienz-Virus (HIV) infizierten Bevölkerung jeden Landes wird mit einer farblichen Kodierung dargestellt. Die Legende in Form einer Farbskala befindet sich unterhalb der Weltkarte.

Darstellung eines HI-Virus mit Struktur seines Genoms und seinen wichtigsten Enzymen und Glykoproteinen (gp120 und gp41)
Bild: „Diagram of the HIV virus“ des US National Institute of Health. Lizenz: Public DomainSexuell:
Parenteral:
Vertikal:

Replikationszyklus des HIV:
1. Virion bindet den CD4-Rezeptor und einen Chemokinrezeptor → Konformationsänderung → ermöglicht Fusion von Virion und der Wirtszelle
2.Uncoating (Freisetzung der Virusgenoms und weiterer Proteine) des Kapsidproteins, sobald das Virion sich im Zytoplasma befindet
3. Durch Reverse Transkriptase vermittelte Synthese proviraler DNA aus viraler RNA
4. Transport viraler DNA in den Zellkern und Integration in die Wirts-DNA mittels Integrase
5. Transkription viraler DNA, Erstellung mehrerer Kopien neuer HIV-RNA und Transport in das Zytoplasma + neue HIV-RNA wird zum Genom neuer Viren + Zytokinaktivierung der Zelle
6. Migration neuer viraler RNA + Proteine + Enzyme an die Zelloberfläche und Ausbildung nicht infektiöser Partikel.
7. Ausknospung von Virusbestandteilen (virale RNA + Proteine) an der Zellmembran aus der Wirtszelle heraus → unreifes HIV. Spaltung neu synthetisierter Polyproteine durch virale Protease → reifes HIV → Freigabe in den Körperkreislauf durch Lyse der Wirtzelle

Mechanismus des Eintritts und der Membranfusion von HIV:
1. Interaktion des gp120 des HIV mit CD4 der Wirtszelle
2. Sekundäre Interaktion mit einem anderen CCR5-Rezeptor → Konformationsänderung an gp120
3. Einbringung der Enden von gp41 in die Zielzellmembran
4. gp41 faltet sich in zwei Hälften und bildet Coiled Coils (gewundene Helices) → Annäherung viraler und zellulärer Membran → Fusion
Akute Phase (Infektion, Ausbreitung, retrovirales Syndrom):
Chronische Phase/klinische Latenz:
AIDS:

Diagramm über die Beziehung von CD4+ T-Zellzahl und Viruslast während des klinischen Verlaufs einer HIV-Infektion und AIDS:
Bei primärer/akuter Infektion (Erstinfektion, Ausbreitung und akutes retrovirales Syndrom) kommt es zur Zunahme der Viruslast (Virämie) bei abnehmenden CD4+ T-Zellen. Diese Periode überdauert mehrere Wochen. In der Phase der klinischen Latenz liegt eine geringe, aber anhaltende Virusreplikation vor und es stellt sich eine allmähliche Abnahme der CD4+ Zellen ein. Der Übergang zum AIDS beschreibt die Folge des Zusammenbruchs der Abwehrkräfte des Wirts, einhergehend mit erschöpften CD4+ T-Zellen und steigender Viruslast. Der Krankheitsprogress prädisponiert für opportunistische Infektionen.
Die Klassifikation des Centers for Disease Control and Prevention (CDC) gibt an, dass die Anzahl der CD4+-T-Lymphozyten:
| Bereiche/Stadien der T-Helfer-Zellen | 1 | 2 | 3 |
|---|---|---|---|
| Klinische Einteilung | CD4+ ≥ 500 Zellen/µl | CD4+ 200–499 Zellen/µl | CD4+ < 200 Zellen/µl* |
| A: Asymptomatisch oder akute HIV-Krankheit oder Lymphadenopathie-Syndrom (LAS) | A1 | A2 | A3 |
| B: Symptomatisch, nicht A oder C | B1 | B2 | B3 |
| C: AIDS, einschließlich opportunistischer Infektionen, neurologischer Erkrankungen und Tumoren | C1 | C2 | C3 |
Akutes retrovirales Syndrom (akute Phase):
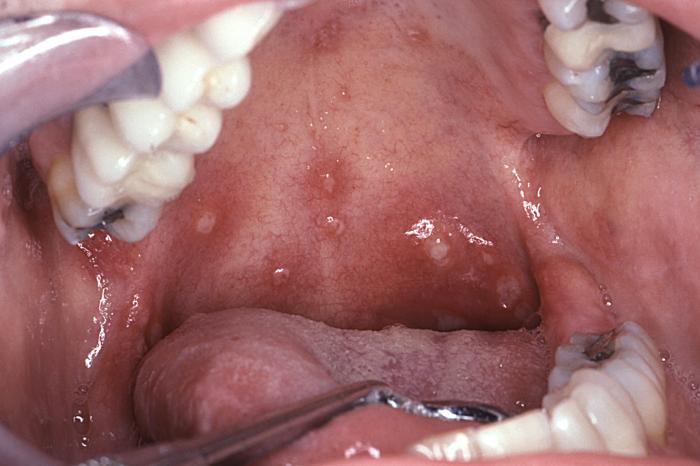
Aphthöse Stomatitis, die typisch für das akute retrovirale Syndrom ist
Bild: „6055“ von CDC/Sol Silverman, Jr., DDS. Lizenz: Public Domain
Virales makulopapulöses Exanthem bei akutem retroviralem Syndrom
Bild: „14925“ von CDC/Dr. Gavin Hart. Lizenz: Public DomainChronische Infektion (klinische Latenz):
AIDS:

Kutane Läsionen eines Kaposi-Sarkoms
Bild: „Kaposi’s sarcoma“ von OpenStax College. Lizenz: CC BY 3.0
Toxoplasmose und AIDS:
Magnetresonanztomographie (MRT) mit ringförmigem Enhancement einer Läsion im Bereich der Capsula interna und des Thalmus bei einem Patienten mit Hemichorea-Hemiballismus

Kryptokokkose:
Röntgenthorax und Computertomographie (CT) zeigen einen solitären Lungenknoten. Die Diagnose einer Kryptokokkose wurde durch eine Biopsie bestätigt.

Mycobacterium avium -Komplex: Untersuchung eines HIV-infizierten Mannes bei schweren rechtsseitigen Oberbauchschmerzen. Unter Therapie entwickelte er einen ausgedehnten, supraklavikulären Lymphknotenabszess. Eine Aspiration zeigte eine MAC.
Bild: „Left supraclavicular abscessed lymph node“ von Department of Internal Medicine, Division of Infectious Diseases, University of Michigan Health System, Ann Arbor, Michigan, USA. Lizenz: CC BY 2.0
Mycobacterium avium-Komplex:
Untersuchung eines HIV-infizierten Mannes bei schweren rechtsseitigen Oberbauchschmerzen. Ein CT-Abdomen zeigte mehrere vergrößerte, nekrotische, intraabdominelle Lymphknoten.
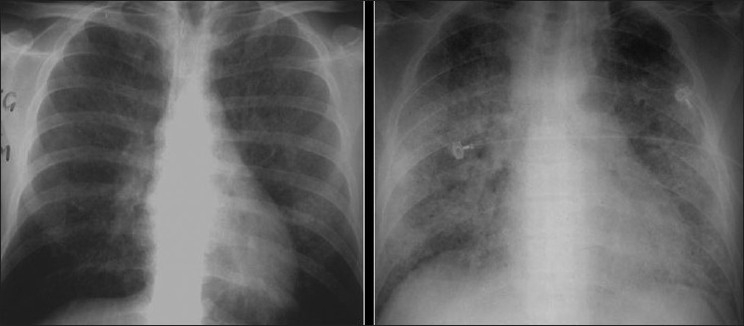
Pneumocystis-Pneumonie:
2 Röntgenaufnahmen des Thorax zeigen ein Milchglas-Phänomen. Der Röntgenbefund des rechten Thorax imitiert ein Lungenödem.

Zu erkennen ist ein Milchglasphänomen mit geographischer bzw. mosaikartiger Verteilung.
Bild: „Pneumocystis carinii pneumonia“ von Annals of Thoracic Medicine. Lizenz: CC BY 4.0
Tuschfärbung bei Cryptococcus:
Zu erkennen ist die Kapsel, die knospende Hefe umgibt.

P. jiroveci :
Methenamin-Silber-Färbung, die Cluster von P. jiroveci -Zysten im Sputum sichtbar macht

Algorithmus zur Diagnostik und Differenzierung zwischen HIV-Infektionen, die entweder durch den Subtyp HIV-1 und HIV-2 ausgelöst wurden
Bild von Lecturio.Aufklärung der Risikogruppen und der Bevölkerung über Infektionsmodus und Prophylaxe: Das
HIV
HIV
Retroviren: HIV wird bevorzugt durch Geschlechtsverkehr oder Kontakt mit infektiösem Blut übertragen.
| Stadium | Alter < 1 Jahr | Alter 1–6 Jahre | Alter ≥ 6 Jahre |
|---|---|---|---|
| 1 | ≥ 1.500 Zellen/µL bzw. ≥ 34 % | ≥ 1.000 Zellen/µL bzw. ≥ 30 % | ≥ 500 Zellen/µL bzw. ≥ 26 % |
| 2 | 750–1.499 Zellen/µl bzw. 26-33 % | 500–999 Zellen/µL bzw. 22-29 % | 200–499 Zellen/µl bzw. 14-25 % |
| 3 (AIDS) | < 750 Zellen/µL bzw. < 26 % | < 500 Zellen/µL bzw. < 22 % | < 200 Zellen/µL bzw. < 14 % |