Das Hodgkin-Lymphom (HL) ist eine maligne Erkrankung der B-Lymphozyten, die ihren Ursprung in den Lymphknoten Lymphknoten Lymphsystem hat. Der pathognomonische histologische Befund des Hodgkin Lymphoms sind Hodgkin/Reed-Sternberg (HRS)-Zellen (riesige, mehrkernige B-Zellen B-Zellen B-Zellen mit eosinophilen Einschlüssen). Die Krankheit manifestiert sich am häufigsten mit Lymphadenopathie Lymphadenopathie Lymphadenopathie (am häufigsten zervikal), Nachtschweiß, Gewichtsverlust und /oder Fieber Fieber Fieber, was unter dem Begriff der B-Symptomatik zusammengefasst wird. Manchmal kommt es außerdem zu Splenomegalie Splenomegalie Splenomegalie und Hepatomegalie. Zu den diagnostischen Tests gehören die histologische Analyse der Lymphknoten Lymphknoten Lymphsystem, in welchen HRS-Zellen erkennbar sind, Labordiagnostik sowie CT- und PET-Scans. Das Hodgkin Lymphom wird stadiengerecht mit Chemotherapie und Bestrahlung behandelt. Die Prognose hat sich mit dem Aufkommen der Chemotherapie deutlich verbessert und ist insgesamt im Vergleich zu anderen Krebserkrankungen sehr gut.
Kostenloser
Download
Lernleitfaden
Medizin ➜
Das Hodgkin-Lymphom (HL) ist ein monoklonales B-Zell-Lymphom (Neoplasma) mit Ursprung in den Lymphknoten Lymphknoten Lymphsystem, bei dem die malignen Hodgkin/Reed-Sternberg (HRS)-Zellen mit einer heterogenen Population nicht-neoplastischer Entzündungszellen vermischt sind.
Basierend auf der WHO-Klassifikation werden HLs in die folgenden Typen und Subtypen nach Immunphänotyp und Morphologie unterteilt.
Klassisches HL (95 %):
Nodulär-lymphozytenprädominantes HL (NLPHL):

Hodgkin-Lymphom: Feinnadelpunktion eines Lymphknotens mit Hodgkin/Reed-Sternberg-Zelle (Mehrkernige Zelle in der Mitte) Bild: „Hodgkin Lymphoma Reed-Sternberg Cell on FNA (45240026874)” von Ed Uthman. Lizenz: CC BY 2.0

Pathognomonischer histologischer Befund beim Hodgkin-Lymphom:
Die Reed-Sternberg-Zelle, „Eulenaugen-Zelle“
Zeitverlauf:
Die häufigsten Symptome:

Hodgkin-Lymphom:
Prominente zervikale Lymphadenopathie
„B“-Symptomatik in 40 % der Fälle vorhanden:
Andere Symptome:
Labordiagnostik:
Bildgebende Verfahren:

Röntgenthorax zeigt mediastinale Lymphadenopathie bei Hodgin-Lymphom
Bild : “Hodgkin’s lymphoma presenting with markedly elevated IgE: a case report” von Ellis AK, Waserman S. Lizenz: CC BY 2.0Biopsie:
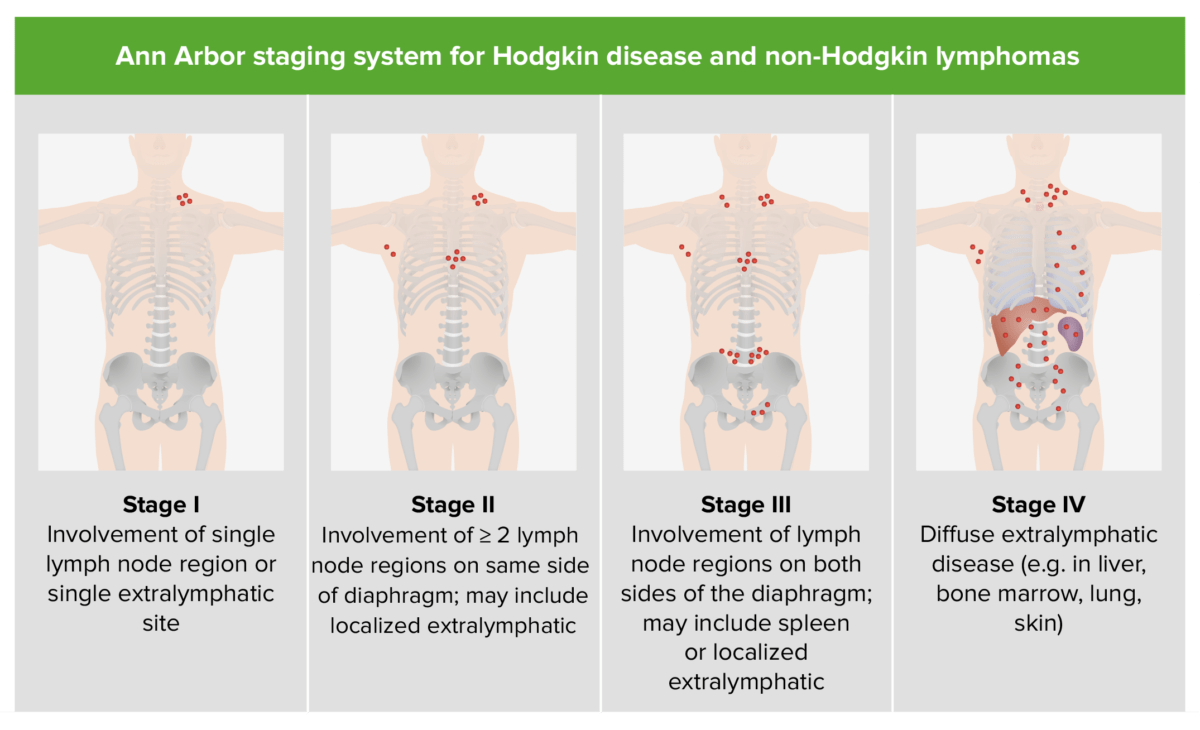
Die Stadieneinteilung basiert auf der Ann-Arbor-Klassifikation.