Das Idiopathsiche Parkinson-Syndrom (IPS) ist eine chronisch fortschreitende neurodegenerative Erkrankung. Obwohl die Ursache unbekannt ist, werden derzeit mehrere genetische und umweltbedingte Risikofaktoren vermutet. Patient*innen weisen klinisch einen Ruhetremor, eine Bradykinese, einen Rigor und eine posturale Instabilität aus. Charakteristisch ist dadurch ein kleinschrittiger, schlurfender Gang. Weitere nicht motorische Symptome sind unter anderem Schlafstörungen, eine Orthostatische Dysregulation, Schmerzen, olfaktorische Störungen und Neuropsychiatrische Symptome wie Depression und Psychosen. Morbus Parkinson wird klinisch anhand charakteristischer Anzeichen und Symptome diagnostiziert. Der postmortale Befund von Lewy-Körperchen im Gehirn ist die einzige sichere Bestätigung für die Krankheit. Die Behandlung umfasst unterstützende körperliche und pyschologische Therapie sowie Medikamente wie Levodopa Levodopa Pharmakotherapie bei Morbus Parkinson/Carbidopa, Monoaminoxidase-Typ-B-Hemmer und Dopaminagonisten.
Kostenloser
Download
Lernleitfaden
Medizin ➜
Das Idiopathische Parkinson-Syndrom (IPS) ist eine chronische, fortschreitende neurodegenerative Erkrankung des ZNS mit den Hauptmerkmalen Ruhetremor, Rigor, Bradykinese und posturale Instabilität.
Die Ätiologie des Morbus Parkinson ist unklar, hängt jedoch von verschiedenen genetischen und umweltbedingten Faktoren ab.
Kompensationsmechanismen im Gehirn können die Auswirkungen des Dopaminmangels vorübergehend verringern, bis diese Mechanismen durch das Fortschreiten der Erkrankung überwältigt werden.
Die Anzeichen von Parkinson sind fortschreitend und treten allmählich über einen langen Zeitraum von Jahren bis Jahrzehnten auf.
Die Diagnose eines Morbus Parkinson wird durch die Anamnese und neurologische Untersuchung gestellt.
Die Diagnose erfordert 4 Kriterien:
Motorischer Parkinsonismus, ein wesentliches Kriterium der Parkinson-Krankheit, erfordert eine Bradykinese und mindestens 1 der folgenden Punkte:
Absolute Ausschlusskriterien (inkompatibel mit einer IPS-Diagnose):
Unterstützende Kriterien:
Warnsignale (Anzeichen einer alternativen Pathologie, die auf eine andere Diagnose hinweisen):
Es gibt keine bildgebende Verfahren oder Labordiagnostik, um die klinische Diagnose Idiopathisches Parkinson-Syndrom zu bestätigen:
Das Idiopathische Parkinson-Syndrom wird erst durch den Befund von Lewy-Körperchen bei der postmortalen Analyse bestätigt.
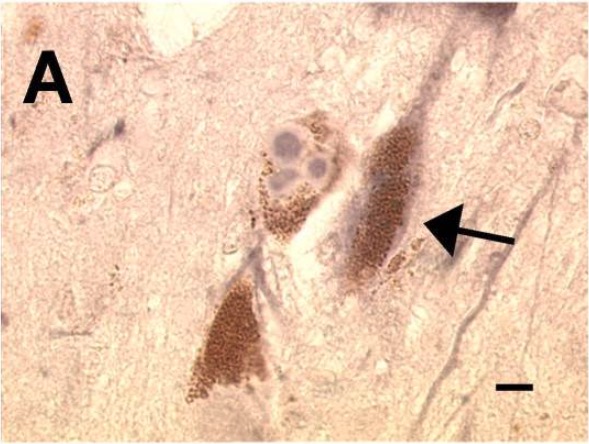
Lewy-Körperchen, wie sie bei einer betroffenen Person mit Morbus Parkinson zu sehen sind
Bild: „Staining of multiple Lewy bodies“ von Division of Neurology, William Beaumont Hospital Research Institute, Royal Oak, MI 48073, USA. Lizenz: CC BY 2.0Ziel der Therapie ist es, die symptomatischen motorischen und nichtmotorischen Merkmale der Erkrankung zu behandeln, um die Lebensqualität zu verbessern.
Allgemeine Maßnahmen:
Konservative Therapie:
Tiefenhirnstimulation:
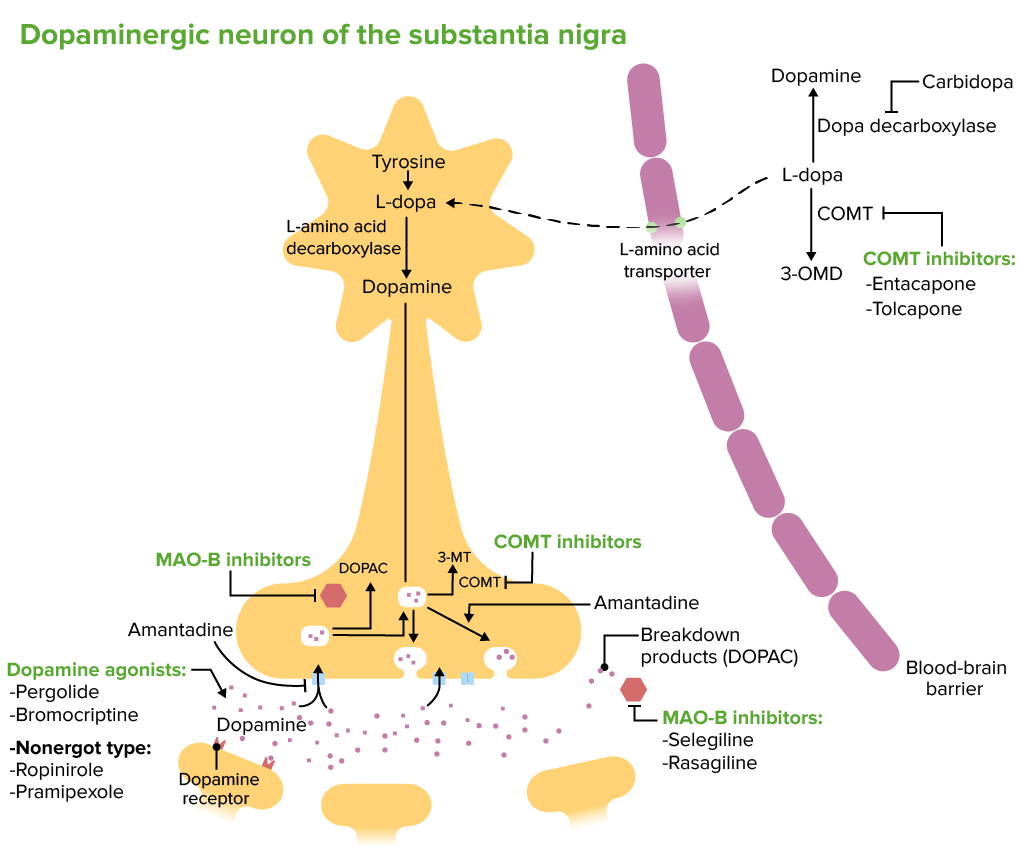
Auswirkungen von Behandlungen der Parkinson-Krankheit auf dopaminerge Neuronen der Substantia nigra 3-OMD:3-O-Methyldopa (ein Metabolit von L-Dopa)
3-MT: 3-Methoxytyramin (ein Metabolit von Dopamin)
COMT: Catechin-O-Methyltransferase (ein Metabolit von Dopamin)
LDOPAC: 3,4-Dihydroxyphenylessigsäure
MAO-B: Monoaminoxidase Typ B